发布日期:2024-12-14 22:59 点击次数:142
俗话说,一朝被蛇咬,十年怕井绳。
这句话我相信大家都听过,类似的事情多少也经历过。
不知道你有没有想过,咱们的大脑为啥会发生这种过激行为。实际上,对于这个现象背后的机制,科学家也所知不多。
近日,由加拿大多伦多大学附属儿童医院Sheena A. Josselyn和Paul W. Frankland,以及卡尔加里大学Matthew N. Hill领衔的研究团队,在顶级期刊《细胞》上发表了一篇重磅研究论文[1],揭示了背后的神经学机制。
他们发现,在急性应激的刺激下,体内糖皮质激素水平会大幅升高,进而诱导神经元释放更多的内源性大麻素,抑制外侧杏仁核中小清蛋白阳性(PV+)神经元的活性,导致下游记忆神经元的激活不能被抑制,因此形成了一个更大的记忆痕迹神经集合体,促进恐惧记忆泛化。
简单来说,原本只需要少数神经元记录的恐惧记忆,被大脑当成一件大事儿记录在更大一片神经元中了。这就导致一有“风吹草动”,恐惧记忆就被激活,造成过度的紧张焦虑。
好消息是,他们还发现,糖皮质激素受体拮抗剂等阻断上述神经通路的药物,可以恢复急性应激小鼠模型的恐惧记忆特异性。这也意味着,创伤后应激障碍(PTSD)和广泛性焦虑障碍有望迎来新疗法。

对于动物而言,恐惧记忆对于生存至关重要,因为它可以帮助我们避免不必要的伤害。
然而,在现实生活中存在一些恐惧记忆过度泛化的现象。举个简单的例子,我们做饭的时候,很容易伤到手,一般而言,在伤到手之后,我们下次看到刀会更加小心谨慎;但如果因此远离厨房,甚至一想到厨房就害怕,就属于恐惧记忆被过度泛化了。
在临床上,恐惧记忆被过度泛化也是创伤后应激障碍(PTSD)和广泛性焦虑障碍等精神疾病的特征。然而,急性应激导致的恐惧记忆过度泛化背后的神经学机制,目前还鲜为人知。
现在已知的是,每个记忆的形成只需要稀疏的神经元参与,整个过程大概可以分成两部分:第一步,兴奋性相对最高的神经元被纳入记忆痕迹集合体;第二步,那些兴奋性较低的神经元,要静息下来,为后续的记忆做准备[2]。
然而,已经有研究发现,如果破坏抑制性神经元(例如PV+神经元),就会导致记忆痕迹集合体变大,参与的神经元过多;而且那些记忆痕迹集合体较大的小鼠会表现出泛化的恐惧记忆,而不是特定的恐惧记忆[3]。
显然,记忆痕迹集合体的变化是揭示恐惧记忆泛化分子机制的突破口。

Josselyn团队先确认了急性应激对恐惧记忆泛化的影响。
他们发现,30分钟的束缚应激(RS)就能让小鼠表现出恐惧记忆泛化,即无法区分危险刺激和安全刺激。
考虑到急性应激会导致糖皮质激素(小鼠体内为皮质酮,CORT)水平增加,他们想知道糖皮质激素是否也参与了急性应激诱导的恐惧记忆泛化。在给小鼠注射糖皮质激素抑制剂之后,束缚应激小鼠的特异性恐惧记忆就恢复了。这说明,糖皮质激素确实参与束缚应激诱导的恐惧记忆泛化。
后续的小鼠研究表明,杏仁外侧核(LA)糖皮质激素受体与恐惧记忆泛化有关,以及3mg/kg的皮质酮(CORT)是诱导恐惧记忆泛化最强烈和最特异的剂量。这也与人体数据一致,说明只有高度紧张的创伤事件才会导致泛化。
此外,他们还发现,恐惧记忆泛化在给予刺激后不久就会发生,而不是像以前的一些研究结果所认为的需要一个潜伏期。
鉴于皮质酮是恐惧记忆泛化的充要条件,在后续的研究中他们就采用注射皮质酮(3mg/kg),来探索急性应激诱发恐惧记忆泛化的分子和神经学机制。
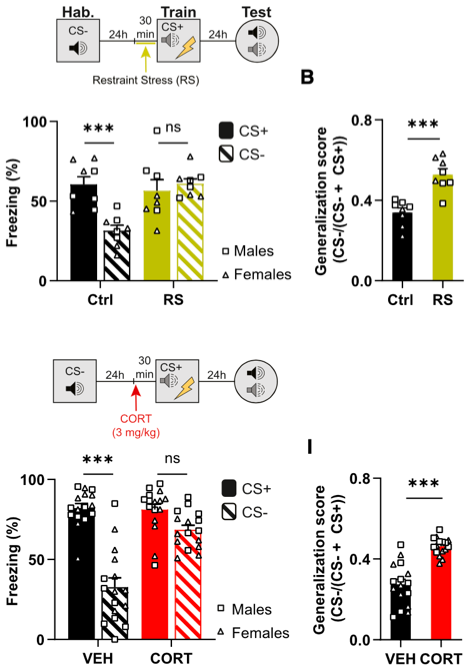
正如Josselyn团队所料,皮质酮处理的小鼠表现出更大的、稀疏程度更低的记忆痕迹集合体。此外,他们还发现,皮质酮影响的是记忆痕迹集合体形成的第二步,即平息兴奋性程度较低的神经元。
简单来说,皮质酮处理让大脑没有处理掉记忆痕迹集合体中兴奋性较低的神经元,所以就导致记忆痕迹集合体扩大了。
由于杏仁外侧核(LA)的小清蛋白阳性(PV+)神经元是抑制性神经元,且是维持记忆痕迹集合体稀疏性的关键神经元,Josselyn团队就观察了皮质酮对PV+神经元活性的影响。
研究结果显示,皮质酮确实特异性地降低了杏仁外侧核PV+神经元的活性,导致杏仁外侧核中兴奋性神经元活性的增加,最终的后果就是恐惧记忆痕迹集合体变得更大且密集。
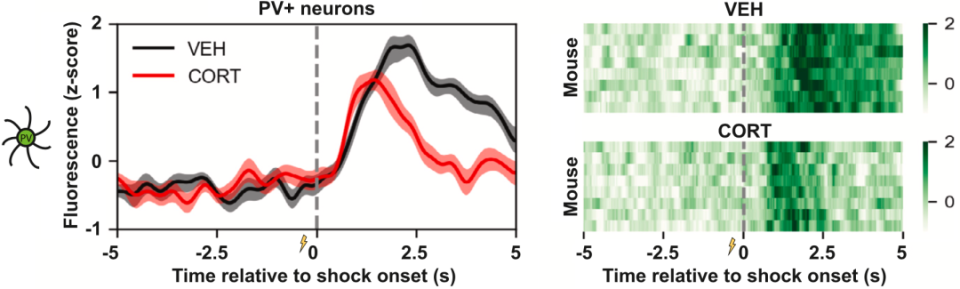
那这一切是如何发生的呢?
在查阅历史文献之后,Josselyn团队发现,皮质酮和急性应激都会诱导包括杏仁核在内的许多脑区快速释放内源性大麻素(eCB),而内源性大麻素的受体CB1Rs又定位于抑制性中间神经元上,激活后可以降低抑制性神经递质γ-氨基丁酸(GABA)的释放。
显然,内源性大麻素和下游信号通路有嫌疑。不过,内源性大麻素主要有两种:花生四烯酸甘油酯(2-AG)和花生四烯酸乙醇胺(AEA)。那么,究竟是谁接了皮质酮的棒呢?
由于与对照组小鼠相比,皮质酮处理或束缚应激(RS)小鼠的杏仁核中2-AG和AEA水平都有所增加,因此得一个个验证二者的作用。
后续分析结果发现,虽然2-AG对恐惧记忆的形成很重要,但它在皮质酮诱导的恐惧记忆泛化中并不发挥特殊作用,AEA对恐惧记忆泛化有特异性影响。简单来说,接棒者是AEA。
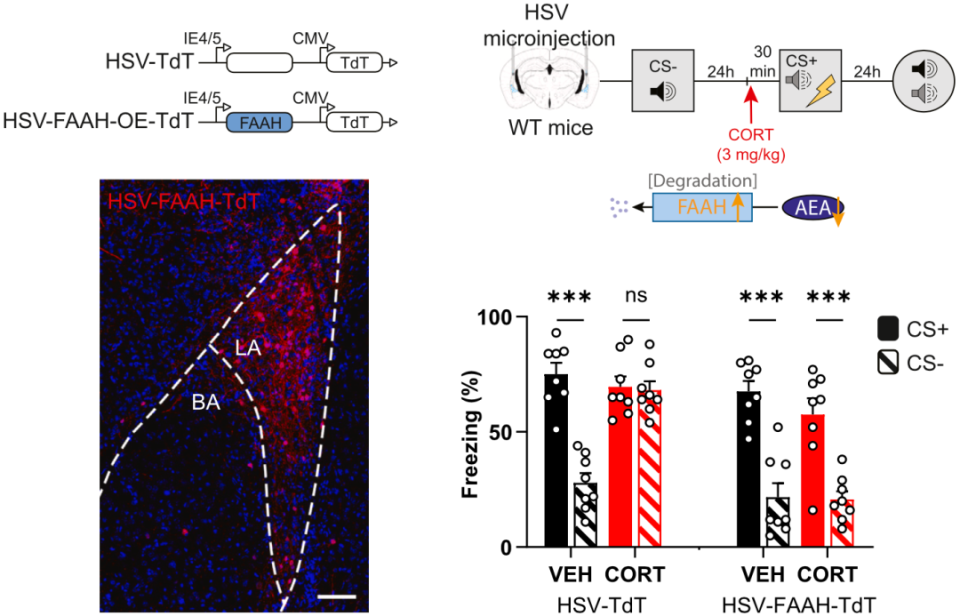
很快,Josselyn团队又证实,杏仁外侧核PV+神经元上确实有AEA的受体CB1Rs。敲除杏仁外侧核PV+神经元的CB1Rs,足以改善束缚应激诱导的恐惧记忆泛化。
至此,急性应激诱导恐惧记忆泛化的分子和神经学通路就打通了。
总体来看,急性应激会诱导皮质酮水平增加,促进杏仁外侧核神经元释放AEA;AEA与PV+神经元上的受体CB1R结合,导致PV+神经元的抑制性神经递质GABA释放减少;破坏了兴奋性程度较低的神经元的平息,从而形成了一个更大、更致密记忆痕迹集合体;最终这一较大的神经集合会被外界特异性和非特异性刺激重新激活,从而形成泛化的恐惧记忆。
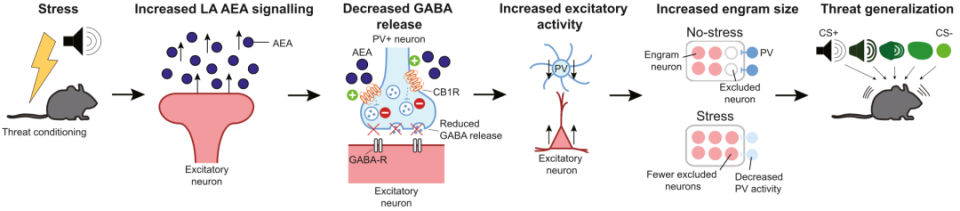
在研究的最后,Josselyn团队还探索了这一发现的临床应用价值。
他们通过给小鼠注射糖皮质激素受体拮抗剂(RU486)或AEA合成抑制剂(LEI-401),发现它们都可以恢复束缚应激小鼠的恐惧记忆特异性。这说明,这两种药物有临床治疗潜力。
期待相关药物尽快推进到临床研究中,以造福广大的创伤后应激障碍(PTSD)和广泛性焦虑障碍患者。